Das Endocannabinoid-System (ECS) ist eines der faszinierendsten und am meisten unterschätzten Regulationssysteme des menschlichen Körpers. Es existiert in nahezu jedem Gewebe — einschließlich der Haut — und steuert grundlegende Prozesse wie Entzündung, Schmerzempfindung, Immunantwort und Zellproliferation. Um zu verstehen, warum CBD auf die Haut wirkt, muss man das ECS verstehen. Dieser Artikel erklärt es von Grund auf: Aufbau, Funktion, retrograde Signalgebung und die besondere Bedeutung des kutanen ECS für Hautgesundheit und CBD-Wirkung.
Inhaltsverzeichnis
- Aufbau: Die drei Kernkomponenten des ECS
- Wie das ECS entdeckt wurde
- Funktion: Retrograde Signalgebung erklärt
- Das kutane ECS: Die Haut als eigenständiges ECS-Organ
- Das ECS als Homöostase-System
- Wie CBD das ECS moduliert
- Klinische Relevanz für die Hautpflege
- Fazit: Das ECS als Ausgangspunkt
- Wissenschaftliche Quellen
1. Aufbau: Die drei Kernkomponenten des ECS
Das Endocannabinoid-System besteht aus drei funktional zusammenhängenden Elementen, die gemeinsam ein präzises Signalnetzwerk bilden: den Endocannabinoiden (körpereigene Signalmoleküle), den Cannabinoid-Rezeptoren (Zielstrukturen auf Zelloberflächen) und den Abbauenzymen (die das Signal beenden und regulieren).

Die Endocannabinoide: Anandamid und 2-AG
Anders als klassische Neurotransmitter werden Endocannabinoide nicht in Vesikeln gespeichert. Sie werden bedarfsgerecht aus Membranphospholipiden synthetisiert — ein Mechanismus, der direkt an die Aktivität der Zelle gekoppelt ist und die retrograde Signalgebung des ECS ermöglicht.
Anandamid (AEA), 1992 von Devane et al. entdeckt und nach dem Sanskritwort ananda (Seligkeit) benannt, bindet bevorzugt an CB1-Rezeptoren und wird rasch durch FAAH abgebaut.[1] 2-Arachidonoylglycerol (2-AG) ist das abundantere Endocannabinoid, bindet an beide Rezeptortypen und wird durch MAGL abgebaut.
CB1 und CB2: Zwei Rezeptoren mit gegensätzlichen Profilen
CB1 dominiert im Zentralnervensystem und vermittelt Schmerz-, Stimmungs- und Gedächtnismodulation — es ist das primäre Ziel von THC. CB2 wurde 1993 von Sean Munro entdeckt und ist hauptsächlich in Immunzellen und peripheren Geweben — darunter der Haut — exprimiert.[2] Diese Trennung erklärt, warum topisches CBD auf die Haut wirken kann, ohne zentralnervöse Effekte zu erzeugen.
FAAH und MAGL: Die Signalbremsen
Die Fettsäureamidhydrolase (FAAH) und die Monoacylglycerollipase (MAGL) beenden das ECS-Signal, indem sie AEA bzw. 2-AG enzymatisch abbauen. CBD hemmt FAAH selektiv — das Ergebnis ist eine verlängerte Anandamid-Verfügbarkeit am Rezeptor. CBD erhöht also nicht direkt die ECS-Aktivität, sondern verlängert die Wirkdauer körpereigener Signale.
2. Wie das ECS entdeckt wurde
Die Geschichte des ECS beginnt mit einer pharmakologischen Frage: Warum wirkt THC im menschlichen Gehirn? In den 1980er Jahren führte diese Frage zur Suche nach spezifischen Bindungsstellen für THC — und zu einer der überraschendsten Entdeckungen der Neurobiologie.
1988 beschrieben Howlett und Devane erstmals Cannabinoid-Bindungsstellen im Rattenhirn. 1990 gelang Lisa Matsuda die Klonierung des CB1-Rezeptors — der Beweis, dass das Gehirn Strukturen besitzt, die evolutionär für Cannabis-ähnliche Moleküle ausgelegt sind. Die entscheidende Folge: Wenn Rezeptoren existieren, müssen körpereigene Liganden existieren. 1992 wurde Anandamid entdeckt.[1]
🔬 Wichtige Einordnung: Das ECS wurde entdeckt, weil man verstehen wollte, wie Cannabis wirkt — nicht umgekehrt. Das ECS existierte Millionen von Jahren vor Cannabis. Es ist kein „Cannabis-System”, sondern ein fundamentales Regulationssystem, das Cannabis zufällig modulieren kann — weil Phytocannabinoide strukturell den körpereigenen Liganden ähneln.
3. Funktion: Retrograde Signalgebung erklärt
Das definierendste Merkmal des ECS ist die retrograde Signalgebung — eine Kommunikationsrichtung, die dem klassischen Neurotransmitter-Modell entgegenläuft. Klassische Neurotransmitter fließen von der präsynaptischen zur postsynaptischen Zelle. Endocannabinoide fließen in die entgegengesetzte Richtung.
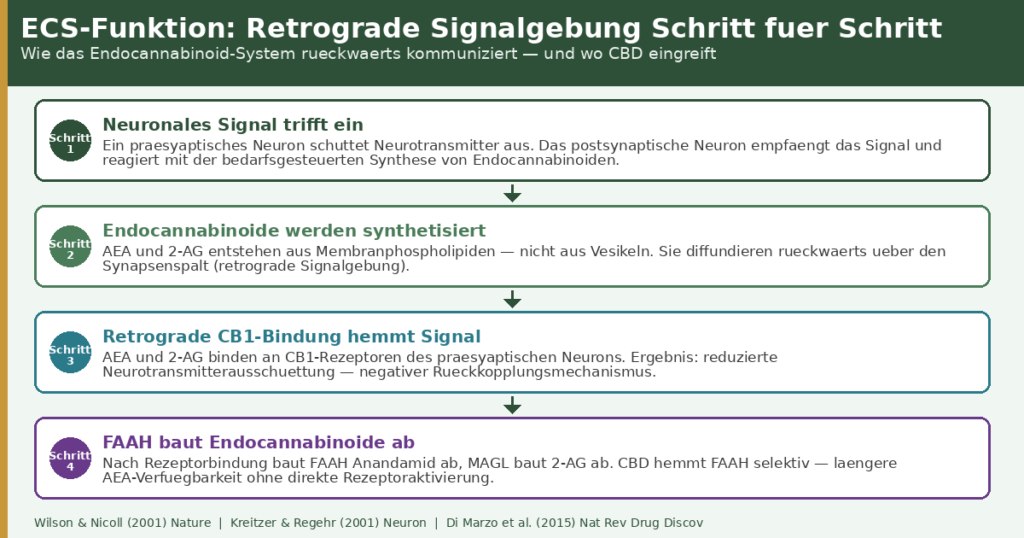
Wilson & Nicoll (2001) beschrieben diesen Mechanismus erstmals systematisch in Nature: Das postsynaptische Neuron antwortet auf eingehende Signale mit der Synthese von Endocannabinoiden, die rückwärts über den Synapsenspalt diffundieren und präsynaptische CB1-Rezeptoren aktivieren — was die weitere Neurotransmitterausschüttung hemmt.[3]
Dieser negative Rückkopplungsmechanismus ist biologisch elegant: Das Empfängerneuron kann die Stärke des eingehenden Signals aktiv regulieren. CBD greift in dieses System ein, indem es FAAH hemmt und damit die Signaldauer von Anandamid verlängert — ohne den Mechanismus zu überwältigen oder zu blockieren.
💡 Warum das pharmakologisch bedeutsam ist: Ein direkter CB1-Agonist (wie THC) aktiviert den Rezeptor unabhängig vom körpereigenen Signal — mit starken, unkontrollierten Effekten. CBD verlängert nur die Wirkung bereits aktiver körpereigener Signale — ein subtilerer, homöostatisch sinnvoller Mechanismus.
4. Das kutane ECS: Die Haut als eigenständiges ECS-Organ
Die Haut besitzt ein vollständiges, autonomes endocannabinoides System. Bíró et al. (2009) beschrieben das kutane ECS in Trends in Pharmacological Sciences als eigenständiges Regulationssystem mit allen ECS-Komponenten — CB1, CB2, Endocannabinoide, FAAH und MAGL — exprimiert in den wichtigsten Hautzellentypen.[4]

Keratinozyten: Das ECS-reichste Hautgewebe
Keratinozyten machen über 90 % der epidermalen Zellen aus und exprimieren ein bemerkenswert breites Rezeptorrepertoire: CB1, CB2, TRPV1 und TRPV4. Sie sind nicht nur Strukturzellen — sie sind aktive Immunregulatoren, die pro-inflammatorische Zytokine produzieren und das dermale Immunsystem steuern. CBD moduliert diese Funktionen über CB2 und TRPV1 mit nachgewiesener Reduktion von IL-1β und COX-2.
Sebozyten: Sebumregulation über das ECS
Die Talgdrüsenzellen (Sebozyten) exprimieren CB2 und TRPV4. Oláh et al. (2014) zeigten erstmals, dass CBD die Lipogenese in menschlichen Sebozyten hemmt und Entzündungsmarker reduziert — ohne normale Hautzellen zu schädigen.[5] Diese Selektivität — Normalisierung überaktiver Sebozyten bei Schonung gesunder Zellen — ist pharmakologisch bemerkenswert.
Immunzellen der Haut: CB2 als Immunregulator
CB2 ist auf T-Zellen, Mastzellen, Langerhans-Zellen und dermalen Makrophagen exprimiert. Seine Aktivierung — durch AEA (über FAAH-Hemmung durch CBD) oder direkte CB2-Modulatoren — führt zur Reduktion pro-inflammatorischer Zytokine und hemmt die Immunzellmigration in entzündetes Gewebe.
5. Das ECS als Homöostase-System
Das übergeordnete Funktionsprinzip des ECS ist Homöostase — die Aufrechterhaltung eines stabilen inneren Gleichgewichts. Di Marzo fasste dieses Prinzip prägnant zusammen: Das ECS reguliert „eat, sleep, relax, forget and protect” — Nahrungsaufnahme, Schlaf, Stressreduktion, Gedächtniskonsolidierung und Immunschutz.[6]

Für die Haut bedeutet das: Das kutane ECS ist nicht reaktiv, sondern proaktiv. Es hält kontinuierlich das mikrobielle Gleichgewicht, die Barrierefunktion und die Immunantwort im Gleichgewicht — und reagiert auf Störungen wie UV-Exposition, Pathogene oder mechanische Verletzung mit gezielter Gegenregulation.
6. Wie CBD das ECS moduliert
CBD ist kein direkter CB1- oder CB2-Agonist — das ist das häufigste Missverständnis in der CBD-Kommunikation. CBD wirkt auf das ECS über mehrere indirekte Wege gleichzeitig:
| CBD-Wirkmechanismus | Zielstruktur | Ergebnis |
|---|---|---|
| FAAH-Hemmung | Abbauenzym für Anandamid | Erhöhte AEA-Verfügbarkeit, indirekte CB2-Aktivierung |
| Negativer allosterischer Modulator | CB1-Rezeptor | Abschwächung von THC-Effekten, Schutz vor CB1-Überaktivierung |
| TRPV1-Agonismus/Desensibilisierung | Schmerzkanal TRPV1 | Kurzfristige Aktivierung, dann Desensibilisierung — funktionale Analgesie |
| PPARγ-Aktivierung | Kernrezeptor für Lipidmetabolismus | Sebumreduktion in Sebozyten, Entzündungshemmung |
| GPR55-Antagonismus | Orphan-Rezeptor | Mögliche Hemmung der Zellproliferation |
Diese Pluripotenz macht CBD pharmakologisch interessant und gleichzeitig schwer zu charakterisieren. Ein einzelner Wirkmechanismus erklärt die beobachteten Effekte nicht vollständig — was die Forschung komplex, aber das therapeutische Potenzial breit macht.
7. Klinische Relevanz für die Hautpflege
Das kutane ECS ist an der Pathophysiologie mehrerer häufiger Hauterkrankungen direkt beteiligt:
- Akne vulgaris: Überaktive Sebozyten, CB2-Dysregulation, erhöhte lokale Entzündung — alle drei Faktoren sind ECS-modulierbar
- Atopische Dermatitis: Veränderte CB1/CB2-Expression in Keratinozyten, erhöhte TRPV1-Aktivität, gestörte Barrierefunktion
- Psoriasis: Hyperproliferation von Keratinozyten, bei der CB1-Aktivierung antiproliferativ wirken kann
- Pruritis (Juckreiz): TRPV1 und CB1 sind direkt an der Juckreiz-Signalgebung beteiligt — topische ECS-Modulation kann lindernd wirken
⚠️ Wissenschaftliche Einschränkung: Die meisten ECS-Hautforschungsstudien wurden in vitro oder an Tiermodellen durchgeführt. Kontrollierte klinische Humanstudien mit topischen CBD-Formulierungen sind noch begrenzt. Die mechanistische Plausibilität ist hoch — klinische Gewissheit erfordert weitere Forschung.
8. Fazit: Das ECS als Ausgangspunkt
Das Endocannabinoid-System ist kein Zubehör zum Verständnis von CBD — es ist der Ausgangspunkt. Ohne ECS-Verständnis bleiben CBD-Wirkungen entweder unverstanden oder werden falsch kommuniziert.
- Das ECS existiert unabhängig von Cannabis. Es ist ein fundamentales Homöostasesystem, das seit Millionen von Jahren aktiv ist — Cannabis moduliert es zufällig.
- CB1 und CB2 haben gegensätzliche Profile. CB1 im ZNS = THC-Wirkung. CB2 in Haut und Immunsystem = CBD-relevante Hautpflegewirkung ohne psychoaktive Effekte.
- CBD ist kein direkter Rezeptor-Agonist. CBD wirkt über FAAH-Hemmung, allosterische CB1-Modulation und Non-CB-Rezeptoren wie TRPV1 und PPARγ.
- Das kutane ECS ist vollständig und autonom. Die Haut besitzt alle ECS-Komponenten und reagiert auf topisches CBD über CB2, TRPV1 und PPARγ in Keratinozyten und Sebozyten.
- Das ECS reguliert Homöostase. Entzündung, Sebum, Barrierefunktion und Immunantwort — das kutane ECS hält sie im Gleichgewicht und ist damit ein legitimes therapeutisches Ziel.
🌿 ECS-informierte Hautpflege von MOAR.
Die CBD-Produkte von MOAR basieren auf den in diesem Artikel beschriebenen ECS-Mechanismen — mit Vollspektrum-Extrakt für maximale Rezeptorabdeckung, CO₂-Extraktion und chargenspezifischem COA. Produkte entdecken →
Wissenschaftliche Quellen
- Devane, W. A., Hanus, L., Breuer, A., Pertwee, R. G., Stevenson, L. A., Griffin, G., … & Mechoulam, R. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science, 258(5090), 1946–1949. doi:10.1126/science.1470919
- Munro, S., Thomas, K. L., & Abu-Shaar, M. (1993). Molecular characterization of a peripheral receptor for cannabinoids. Nature, 365(6441), 61–65. doi:10.1038/365061a0
- Wilson, R. I., & Nicoll, R. A. (2001). Endogenous cannabinoids mediate retrograde signalling at hippocampal synapses. Nature, 410(6828), 588–592. doi:10.1038/35069076
- Bíró, T., Tóth, B. I., Haskó, G., Paus, R., & Pacher, P. (2009). The endocannabinoid system of the skin in health and disease. Trends in Pharmacological Sciences, 30(8), 411–420. doi:10.1016/j.tips.2009.05.004
- Oláh, A., Tóth, B. I., Borbíró, I., Sugawara, K., Szöllősi, A. G., Czifra, G., … & Bíró, T. (2014). Cannabidiol exerts sebostatic and antiinflammatory effects on human sebocytes. Journal of Clinical Investigation, 124(9), 3713–3724. doi:10.1172/JCI64628
- Di Marzo, V. (2008). Targeting the endocannabinoid system: to enhance or reduce? Nature Reviews Drug Discovery, 7(5), 438–455. doi:10.1038/nrd2553
- Tóth, K. F., Ádám, D., Bíró, T., & Oláh, A. (2019). Cannabinoid Signaling in the Skin: Therapeutic Potential of the “C(ut)annabinoid” System. Molecules, 24(5), 918. doi:10.3390/molecules24050918
Dieser Artikel dient ausschließlich zu Bildungs- und Informationszwecken und stellt keine medizinische Beratung dar. Die beschriebenen Produkte sind keine Arzneimittel.