Auf immer mehr CBD-Produkten steht es: „EU-GMP-zertifiziert” oder „nach GMP-Standards hergestellt”. Aber was bedeutet das wirklich — und warum solltest du als Verbraucher darauf achten? GMP steht für Good Manufacturing Practice, die Gute Herstellungspraxis — und sie ist der strengste Produktionsstandard, dem ein CBD-Hersteller freiwillig unterliegen kann. Dieser Artikel erklärt, was dahintersteckt, was er dir garantiert und wo die Grenzen liegen.
Inhaltsverzeichnis
- Was ist EU-GMP? Ursprung und Grundprinzipien
- Was EU-GMP konkret regelt
- GMP-zertifiziert vs. nicht zertifiziert
- GMP in der CBD-Produktion: Vier Qualitätsschritte
- GMP und andere Qualitätsstandards im Vergleich
- GMP und das COA: Der Zusammenhang
- Was GMP für dich als Verbraucher bedeutet
- Fazit: GMP als Mindestanforderung verstehen
- Wissenschaftliche Quellen und Rechtsgrundlagen
1. Was ist EU-GMP? Ursprung und Grundprinzipien
Die Gute Herstellungspraxis (GMP — Good Manufacturing Practice) ist ein international anerkanntes Regelwerk für die Herstellung von Arzneimitteln, Medizinprodukten und bestimmten Lebensmittel- und Kosmetikinhaltsstoffen. In der Europäischen Union ist GMP für Humanarzneimittel durch die Richtlinie 2003/94/EG verbindlich geregelt — ausgeführt im EudraLex Volume 4, dem umfassenden EU-GMP-Leitfaden der Europäischen Kommission.[1]
GMP entstand aus einer einfachen Erkenntnis: Laboranalysen am Endprodukt allein können Qualität nicht garantieren. Eine Charge kann alle Tests bestehen und trotzdem Mängel aufweisen, die zufällig unentdeckt blieben. GMP löst dieses Problem anders: Es stellt sicher, dass der Prozess der Herstellung so kontrolliert, dokumentiert und validiert ist, dass Qualität kein Zufallsergebnis ist, sondern ein systematisch reproduziertes Ergebnis.


🔬 Historischer Kontext: GMP wurde in seiner modernen Form nach dem Contergan-Skandal der 1960er Jahre entwickelt — einem der schlimmsten Arzneimittelunglücke der Geschichte, das direkt auf unzureichende Produktionskontrollen zurückzuführen war. Seitdem gilt: Qualität muss in den Prozess eingebaut werden, nicht nachträglich hineingeprüft werden. Dieses Prinzip trägt alle GMP-Regelwerke bis heute.
2. Was EU-GMP konkret regelt
Der EudraLex Volume 4 umfasst neun Kapitel mit präzisen Anforderungen an jeden Aspekt der pharmazeutischen Produktion. Die für CBD-Hersteller relevantesten Bereiche:
Räumlichkeiten und Ausrüstung (Kapitel 3)
Produktionsräume müssen für ihre Zwecke geplant, gebaut und instand gehalten werden. Das bedeutet definierte Reinraumklassen, validierte Klimaanlagen, kontrollierte Temperatur und Feuchtigkeit, klare Trennung von Produktionszonen zur Vermeidung von Kreuzkontaminationen und regelmäßige qualifizierte Wartung aller Produktionsanlagen.
Dokumentation (Kapitel 4)
Jeder Produktionsschritt wird lückenlos schriftlich erfasst. Chargenbücher dokumentieren jeden Rohstoffeingang, jede Produktionsphase und jede Qualitätsprüfung. Abweichungen von Standardverfahren werden erfasst, analysiert und bewertet. Das Grundprinzip: „Wenn es nicht dokumentiert ist, hat es nicht stattgefunden.”
Qualitätskontrolle (Kapitel 6)
Eine unabhängige Qualitätskontrollabteilung (QC) prüft Rohstoffe, Zwischenprodukte und Endprodukte. Die QC-Abteilung darf nicht der Produktion unterstellt sein — strukturelle Unabhängigkeit ist Pflicht. Keine Charge wird ohne bestandene QC-Freigabe in den Handel gebracht.
Validierung (Kapitel 5 und Anhang 15)
Produktionsprozesse und Reinigungsverfahren müssen validiert sein — das heißt: durch dokumentierte Versuche nachgewiesen, dass sie reproduzierbar das gewünschte Ergebnis liefern. Validierung ist nicht einmalig; sie wird bei Prozessänderungen wiederholt und regelmäßig überprüft.
3. GMP-zertifiziert vs. nicht zertifiziert
Der Unterschied zwischen einem GMP-zertifizierten und einem nicht zertifizierten Hersteller ist nicht akademisch — er hat direkte Auswirkungen auf die Produktqualität und Verbrauchersicherheit.

Ein besonders wichtiger Aspekt ist die externe Aufsicht: GMP-zertifizierte Betriebe werden regelmäßig von nationalen Arzneimittelbehörden (in Deutschland: das BfArM, in Österreich: AGES) inspiziert. Die Inspektion ist unangekündigt oder mit kurzem Vorlauf — und kann zur Aussetzung der GMP-Zulassung führen, wenn Mängel festgestellt werden. Das ist ein Anreizrahmen, den kein selbstdeklariierter Standard bieten kann.
⚠️ Achtung bei GMP-Behauptungen: Nicht jede GMP-Behauptung auf einem CBD-Produkt ist gleichwertig. „Nach GMP-Standards hergestellt” kann bedeuten, dass der Hersteller interne Richtlinien befolgt, ohne externe Zertifizierung oder Behördeninspektion. Eine echte EU-GMP-Zertifizierung ist durch eine behördlich ausgestellte Herstellungserlaubnis nachweisbar — frag bei Bedarf danach.
4. GMP in der CBD-Produktion: Vier Qualitätsschritte
CBD-Produkte fallen je nach Klassifizierung (Nahrungsergänzungsmittel, Novel Food, Kosmetikum oder Arzneimittel) unter unterschiedliche regulatorische Anforderungen. GMP-Zertifizierung ist für CBD-Kosmetika und Nahrungsergänzungsmittel nicht gesetzlich vorgeschrieben — sie ist ein freiwilliger Standard, der über die Mindestanforderungen hinausgeht. Genau deshalb ist sie aussagekräftig.
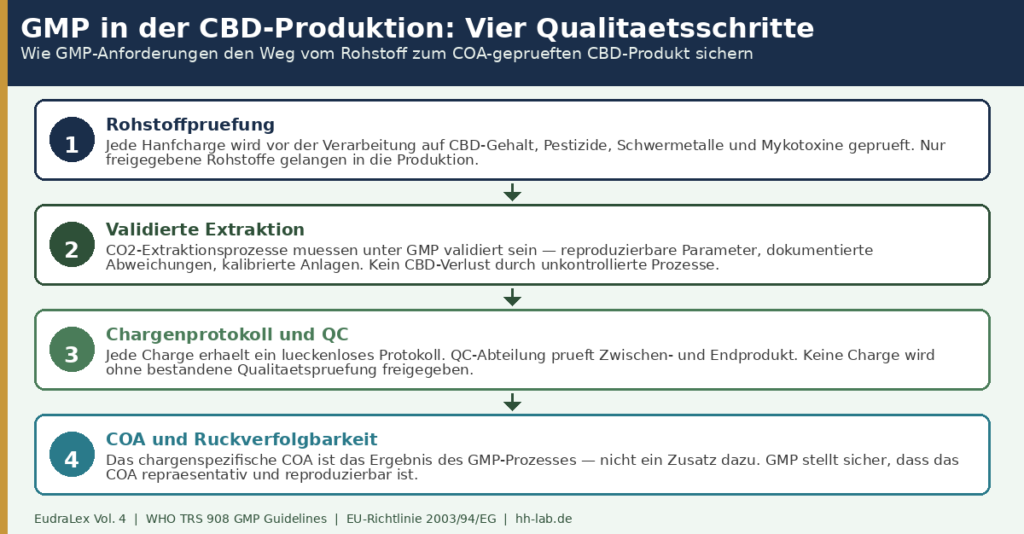
Schritt 1: Rohstoffprüfung vor der Verarbeitung
Jede Hanfcharge, die in die Produktion eingeht, wird vor der Verarbeitung analytisch geprüft: CBD-Gehalt, THC-Wert, Pestizide nach EU-VO 396/2005, Schwermetalle nach Ph. Eur. 2.4.20 und Mykotoxine. Nur Chargen, die alle Spezifikationen erfüllen, werden freigegeben. Nicht konforme Rohstoffe werden zurückgewiesen und dokumentiert.
Schritt 2: Validierte CO₂-Extraktion
Der Extraktionsprozess muss unter GMP validiert sein: reproduzierbare Parameter (Druck, Temperatur, Durchfluss), kalibrierte Anlagen, dokumentierte Abweichungen. Das stellt sicher, dass jede Charge mit identischer Prozessqualität produziert wird — kein CBD-Verlust durch unkontrollierte Prozessführung, keine Chargenunterschiede durch unvalidierte Verfahren.
Schritt 3: Chargenprotokoll und QC-Freigabe
Jede Produktionscharge erhält ein lückenloses Chargenprotokoll, das alle Herstellungsschritte, Zwischenergebnisse und Prüfwerte dokumentiert. Die unabhängige QC-Abteilung prüft das Endprodukt gegen alle Spezifikationen und gibt die Charge frei — oder sperrt sie bei Abweichungen.
Schritt 4: COA als GMP-Ergebnis
Das chargenspezifische Certificate of Analysis (COA) ist das Ergebnis des GMP-Prozesses, nicht ein Zusatz dazu. Unter GMP ist das COA nicht optional — es ist das dokumentierte Beleg der QC-Freigabe. Ein COA ohne GMP-Hintergrund kann valide sein; ein COA mit GMP-Hintergrund ist systematisch abgesichert.
5. GMP und andere Qualitätsstandards im Vergleich
Der CBD-Markt verwendet viele Qualitätsbegriffe. Eine sachliche Einordnung hilft bei der Bewertung.
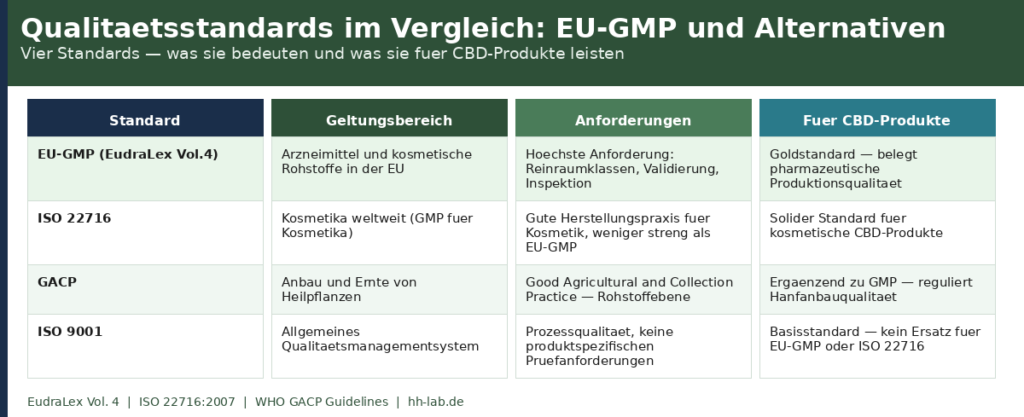
Die wichtigsten Unterschiede in der Praxis: EU-GMP ist der einzige Standard, der externe Behördeninspektionen und eine behördlich ausgestellte Herstellungserlaubnis erfordert. ISO 22716 (GMP für Kosmetika) ist der zweitstärkste Standard — relevant für topische CBD-Produkte wie Cremes und Deodorants. GACP regelt den Anbau, nicht die Verarbeitung. ISO 9001 ist ein allgemeines Qualitätsmanagementsystem ohne produktspezifische Prüfanforderungen.
6. GMP und das COA: Der Zusammenhang
Viele Verbraucher kennen das COA als Qualitätsdokument — weniger bekannt ist, wie es mit GMP zusammenhängt. Vereinfacht gesagt: GMP ist die Produktionsbedingung, das COA ist ihr analytischer Nachweis.
Unter GMP-Bedingungen ist das COA das Ergebnis eines systematischen, behördenüberwachten Prozesses:
- Das analysierende Labor muss nach ISO/IEC 17025 akkreditiert sein
- Analysemethoden müssen validiert und dokumentiert sein
- Die Chargennummer auf dem COA muss identisch mit der auf dem Produkt sein
- Das COA-Ergebnis löst die QC-Freigabe aus — keine Freigabe ohne bestandene Analyse
Ein COA ohne GMP-Hintergrund kann trotzdem valide und informativ sein — wenn es von einem akkreditierten Drittlabor mit korrekter Chargenzuordnung erstellt wurde. Der Unterschied liegt in der systematischen Absicherung: Unter GMP ist das COA ein Pflichtbestandteil eines überwachten Gesamtprozesses. Ohne GMP ist es eine einzelne Analyse, deren Repräsentativität für die gesamte Charge nicht strukturell garantiert wird.
💡 Praxis-Tipp: Wenn ein Hersteller EU-GMP-Zertifizierung beansprucht, kannst du nach der Herstellungserlaubnisnummer fragen. Diese wird von nationalen Arzneimittelbehörden ausgestellt und ist öffentlich einsehbar — z. B. über die EudraGMDP-Datenbank der Europäischen Arzneimittelagentur (EMA).
7. Was GMP für dich als Verbraucher bedeutet
Die ehrliche Antwort: GMP allein macht ein CBD-Produkt nicht automatisch besser wirksam als ein nicht-GMP-Produkt. Was GMP leistet, ist etwas anderes und mindestens ebenso wichtig: Reproduzierbarkeit und Rückverfolgbarkeit.
| Was GMP garantiert | Was GMP nicht garantiert |
|---|---|
| Jede Charge wird unter identischen, validierten Bedingungen hergestellt | Dass das Produkt bei dir wirkt |
| Jede Charge ist vollständig dokumentiert und rückverfolgbar | Dass die Wirkaussagen wissenschaftlich belegt sind |
| Rohstoffe wurden vor der Verarbeitung analytisch geprüft | Dass der CBD-Gehalt optimal für deine Anwendung ist |
| Das COA ist repräsentativ für die Gesamtcharge | Dass keine Wechselwirkungen mit Medikamenten bestehen |
| Externe Behördenaufsicht und regelmäßige Inspektion | Dass das Produkt deine individuelle Fragestellung löst |
Für Verbraucher ist GMP ein starkes Signal für Seriosität und Produktionskonsistenz — besonders relevant für Menschen, die CBD regelmäßig und in konstanter Dosis verwenden. Wer heute eine Charge kauft und in drei Monaten die nächste, will sicher sein, dass beide denselben CBD-Gehalt haben. GMP ist die strukturelle Garantie dafür.
8. Fazit: GMP als Mindestanforderung verstehen
EU-GMP ist kein Marketingbegriff — es ist ein behördlich regulierter, inspektionspflichtiger Produktionsstandard mit jahrzehntelanger Geschichte in der Arzneimittelherstellung. Für CBD-Produkte, die freiwillig unter GMP produziert werden, bedeutet das: höchste Produktionskonsistenz, lückenlose Rückverfolgbarkeit und externe Qualitätsaufsicht.
- GMP bedeutet Prozessqualität, nicht Produktqualität allein. Qualität wird in den Herstellungsprozess eingebaut — nicht nachträglich hineingeprüft.
- EU-GMP erfordert behördliche Herstellungserlaubnis und Inspektion. Nicht jede GMP-Behauptung entspricht diesem Standard — frag nach der Erlaubnisnummer.
- Das COA unter GMP ist Teil eines überwachten Gesamtprozesses. Es belegt nicht nur das Analyseergebnis, sondern die Qualitätssicherung der Gesamtcharge.
- ISO 22716 ist der relevante Standard für CBD-Kosmetika. Für topische CBD-Produkte ist ISO 22716 (GMP für Kosmetika) der passende und aussagekräftige Standard.
- GMP ist Mindestanforderung, kein Alleinstellungsmerkmal. Ein GMP-zertifiziertes Produkt ohne COA, ohne mg/ml-Angabe und ohne Bio-Zertifizierung ist trotzdem unvollständig. GMP ist ein Baustein — nicht das vollständige Qualitätsbild.
🌿 Transparente Produktion bei MOAR.
Die CBD-Produkte von MOAR werden nach den in diesem Artikel beschriebenen Qualitätsprinzipien produziert — mit chargenspezifischem COA, vollständiger INCI-Deklaration und EU-Bio-zertifiziertem Hanf. Produkte ansehen →
Rechtsgrundlagen und Quellen
- Europäisches Parlament und Rat der Europäischen Union. (2003). Richtlinie 2003/94/EG über die Grundsätze und Leitlinien der Guten Herstellungspraxis für Humanarzneimittel und für zur Anwendung beim Menschen bestimmte Prüfpräparate. EUR-Lex
- Europäische Kommission. (2022). EudraLex — Volume 4: Good Manufacturing Practice (GMP) Guidelines. ec.europa.eu
- Europäische Arzneimittelagentur (EMA). (2023). Good Manufacturing Practice. ema.europa.eu
- World Health Organization. (2003). WHO Technical Report Series 908: Good Manufacturing Practices for Pharmaceutical Products. WHO Press. who.int
- International Organization for Standardization. (2007). ISO 22716:2007 — Cosmetics — Good Manufacturing Practices (GMP). iso.org
- European Industrial Hemp Association (EIHA). (2023). GACP for hemp: Good Agricultural and Collection Practices. eiha.org
Dieser Artikel dient ausschließlich zu Informations- und Bildungszwecken. Er stellt keine rechtliche Beratung dar. Für verbindliche Auskünfte zu GMP-Anforderungen wende dich an die zuständige nationale Arzneimittelbehörde. Die beschriebenen Produkte sind keine Arzneimittel.