Wenn Menschen fragen, warum CBD wirkt, beginnen die meisten Antworten mit dem falschen Satz: „CBD bindet an Cannabinoid-Rezeptoren.” Das stimmt nur zur Hälfte — und die andere Hälfte ist pharmakologisch entscheidend. Die vollständige Antwort liegt im Endocannabinoid-System (ECS): einem der komplexesten und weitverzweigtesten Signalsysteme des menschlichen Körpers, das lange vor der Entdeckung von Cannabis existierte — und für das CBD nur ein Modulierungswerkzeug ist, kein Schlüssel.
Dieses Grundlagenkapitel erklärt das ECS von Grund auf: Was es ist, wie es funktioniert, warum es in fast jedem Gewebe des Körpers aktiv ist — und warum du es verstehen musst, um CBD-Wirkungen überhaupt sinnvoll einordnen zu können.
Inhaltsverzeichnis
- Die Entdeckung: Wie das ECS gefunden wurde
- Die drei Kernkomponenten des ECS
- Retrograde Signalgebung: Wie das ECS rückwärts kommuniziert
- Wie CBD das ECS beeinflusst — und wie nicht
- Das ECS in verschiedenen Organsystemen
- Das ECS als Homöostase-System
- Klinische Endocannabinoid-Defizienz: Eine neue Hypothese
- Fazit: Warum das ECS der Ausgangspunkt ist
- Wissenschaftliche Quellen
1. Die Entdeckung: Wie das ECS gefunden wurde
Die Geschichte des ECS beginnt paradoxerweise mit der Frage, warum Cannabis den Menschen beeinflusst. In den 1980er Jahren begannen Neurowissenschaftler, nach spezifischen Bindungsstellen für THC (Tetrahydrocannabinol) im menschlichen Gehirn zu suchen — nach der Logik, dass ein Wirkstoff nur dann wirkt, wenn er an einen spezifischen Rezeptor bindet.
Allyn Howlett und William Devane entdeckten 1988 die ersten Hinweise auf Cannabinoid-Bindungsstellen im Rattenhirn. 1990 klonierten Lisa Matsuda und ihre Kollegen erstmals den CB1-Rezeptor — und bestätigten damit, dass das Gehirn Strukturen besitzt, die evolutionär dafür ausgelegt sind, mit Cannabis-ähnlichen Molekülen zu interagieren.[1]
Die entscheidende Folgefrage war offensichtlich: Wenn der Körper Rezeptoren für Pflanzenmoleküle besitzt — produziert er dann auch körpereigene Liganden für diese Rezeptoren? Die Antwort war ja: 1992 entdeckten Devane et al. Anandamid (AEA) — das erste bekannte körpereigene Endocannabinoid, benannt nach dem Sanskritwort ananda (Seligkeit).[2]
🔬 Historischer Kontext: Das ECS wurde entdeckt, weil man verstehen wollte, wie Cannabis wirkt — nicht umgekehrt. Das bedeutet: Das ECS existierte Millionen von Jahren vor Cannabis, vor CBD, vor jeglicher menschlicher Nutzung der Pflanze. Es ist kein „Cannabis-System” — es ist ein fundamentales Regulationssystem, das Cannabis zufällig modulieren kann.
2. Die drei Kernkomponenten des ECS
Das endocannabinoide System besteht aus drei funktional zusammenhängenden Elementen: den Endocannabinoiden (den körpereigenen Signalmolekülen), den Cannabinoid-Rezeptoren (den Zielstrukturen) und den Abbauenzymen (die das Signal beenden).

Die Endocannabinoide: Anandamid und 2-AG
Im Gegensatz zu klassischen Neurotransmittern werden Endocannabinoide nicht in Vesikeln gespeichert und auf Abruf ausgeschüttet. Sie werden bedarfsgerecht aus Membranphospholipiden synthetisiert — ein einzigartiger Mechanismus, der für die retrograde Signalgebung des ECS entscheidend ist (→ Abschnitt 3).
Anandamid (AEA) wurde 1992 entdeckt und bindet bevorzugt an CB1-Rezeptoren. Es ist lipophil, kurzlebig und wird rasch durch FAAH abgebaut. 2-Arachidonoylglycerol (2-AG) ist das abundantere Endocannabinoid — mit höherer Konzentration im Gewebe und Affinität zu beiden Rezeptortypen (CB1 und CB2). Es wird durch MAGL (Monoacylglycerollipase) abgebaut.
CB1 und CB2: Zwei Rezeptoren, zwei Profile
Sean Munro entdeckte 1993 den CB2-Rezeptor — strukturell ähnlich zu CB1, aber fundamental unterschiedlich in seiner Verteilung und Funktion.[3] Während CB1 im Zentralnervensystem dominiert, ist CB2 primär in peripheren Immunzellen und Haut aktiv. Diese Unterscheidung ist für die CBD-Forschung entscheidend: CBD-Wirkungen auf die Haut laufen primär über das CB2-System — ohne zentralnervöse Effekte.
3. Retrograde Signalgebung: Wie das ECS rückwärts kommuniziert
Die retrograde Signalgebung ist das definierendste und ungewöhnlichste Merkmal des ECS — und gleichzeitig das am häufigsten übersehene in populärwissenschaftlichen CBD-Erklärungen. Klassische Neurotransmitter fließen von der präsynaptischen zur postsynaptischen Nervenzelle. Endocannabinoide fließen in die entgegengesetzte Richtung.
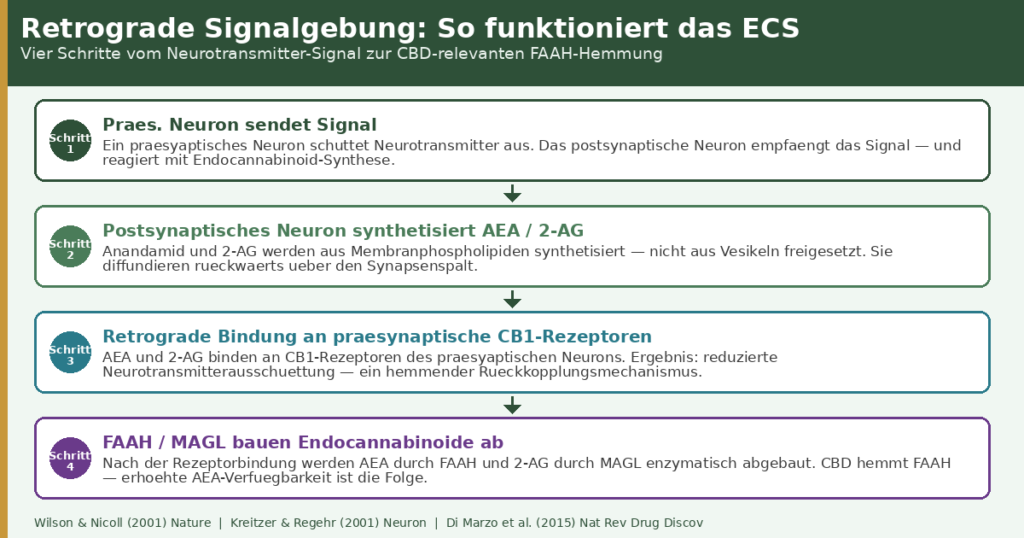
Wilson & Nicoll (2001) beschrieben diesen Mechanismus erstmals systematisch: Das postsynaptische Neuron antwortet auf eingehende Signale, indem es Endocannabinoide synthetisiert und diese rückwärts über den Synapsenspalt schickt — wo sie präsynaptische CB1-Rezeptoren aktivieren und die weitere Neurotransmitterausschüttung hemmen.[4] Es handelt sich um einen eleganten negativen Rückkopplungsmechanismus: Das Empfängerneuron kann die Stärke des eingehenden Signals regulieren.
💡 Warum das für CBD relevant ist: CBD hemmt das Enzym FAAH, das Anandamid abbaut. Das Ergebnis: mehr Anandamid am Rezeptor, länger. CBD erhöht also nicht direkt die ECS-Aktivität — es verlängert die Signaldauer eines bereits aktiven körpereigenen Systems. Das ist pharmakologisch subtiler und homöostatisch sinnvoller als direkte Rezeptoragonismus.
4. Wie CBD das ECS beeinflusst — und wie nicht
Das häufigste Missverständnis über CBD: dass es wie THC direkt an CB1- und CB2-Rezeptoren bindet und diese aktiviert. Das ist falsch — und die Unterscheidung ist klinisch bedeutsam.

CBD als negativer allosterischer Modulator
Laprairie et al. (2015) zeigten, dass CBD an einer anderen Bindungsstelle des CB1-Rezeptors andockt als THC — einer sogenannten allosterischen Stelle. CBD verändert damit die Rezeptorgeometrie so, dass THC und körpereigene Endocannabinoide weniger stark binden können. Das erklärt, warum CBD die psychoaktiven Effekte von THC bei gleichzeitiger Einnahme abschwächt — nicht durch Konkurrenz um dieselbe Bindungsstelle, sondern durch Konformationsänderung des Rezeptors.[5]
CBDs pluripotentes Wirkprofil
CBD ist kein einzieliger Wirkstoff. Neben der FAAH-Hemmung (indirekter CB2-Effekt über AEA) wirkt es auf:
- TRPV1 (Vanilloid-Rezeptor): Schmerz- und Wärmekanal — CBD aktiviert und desensibilisiert ihn
- PPARγ (Kernrezeptor): Lipidmetabolismus und Entzündungsregulation in Keratinozyten und Sebozyten
- GPR55 (Orphan-Rezeptor): CBD wirkt als Antagonist — mögliche Rolle bei Zellproliferation
- 5-HT1A (Serotoninrezeptor): Möglicherweise anxiolytische Wirkung von CBD
5. Das ECS in verschiedenen Organsystemen
Das ECS ist kein Gehirnsystem — es ist ein ubiquitäres Regulationssystem, das in nahezu jedem Gewebe des menschlichen Körpers aktiv ist. Diese Verteilung erklärt, warum CBD so vielfältige potenzielle Wirkungen hat — und warum eine simplistische Erklärung immer zu kurz greift.

Das kutane ECS der Haut
Bíró et al. (2009) beschrieben das kutane ECS als vollständiges, autonomes Regulationssystem der Haut — mit CB1 in sensorischen Neuronen und Haarfollikeln, CB2 in Keratinozyten und Immunzellen sowie TRPV1 und PPARγ als erweiterte Zielstrukturen.[6] Das kutane ECS reguliert Zelldifferenzierung, Apoptose, Proliferation, Immunantwort und Barrierefunktion — und macht die Haut zu einem der therapeutisch interessantesten ECS-Zielgewebe.
6. Das ECS als Homöostase-System
Das übergeordnete Funktionsprinzip des ECS ist Homöostase: die Aufrechterhaltung eines stabilen inneren Milieus angesichts konstant wechselnder äußerer Bedingungen. Di Marzo formulierte dieses Prinzip prägnant: Das ECS ist dafür zuständig, „eat, sleep, relax, forget and protect” zu regulieren — Nahrungsaufnahme, Schlaf, Stressreduktion, Gedächtniskonsolidierung und Immunschutz.[7]
Was das für CBD bedeutet: CBD wirkt nicht isoliert auf einzelne Symptome — es moduliert ein System, das auf Gleichgewicht ausgelegt ist. Das erklärt sowohl die Vielfalt potenzieller CBD-Wirkungen als auch ihre Grenzen: Ein gut funktionierendes ECS profitiert wenig von zusätzlicher CBD-Modulation. Ein dysreguliertes ECS kann durch CBD-Einflüsse in Richtung Gleichgewicht bewegt werden.
| ECS-Funktion | Organsystem | Relevante CBD-Wirkung |
|---|---|---|
| Entzündungsregulation | Haut, Immunsystem | CB2-Modulation, NF-κB-Suppression, IL-Reduktion |
| Schmerzmodulation | Peripheres Nervensystem | TRPV1-Desensibilisierung, CB1-Modulation |
| Sebumregulation | Talgdrüsen (Sebozyten) | PPARγ-Aktivierung, Lipogenese-Hemmung |
| Stimmungsregulation | ZNS (Hippocampus, Amygdala) | Indirekte AEA-Erhöhung, 5-HT1A-Aktivierung |
| Immunhomöostase | Lymphozyten, Makrophagen | CB2-Agonismus via AEA, Zytokinmodulation |
7. Klinische Endocannabinoid-Defizienz: Eine neue Hypothese
Russo (2016) entwickelte in einer viel diskutierten Arbeit die Hypothese der Clinical Endocannabinoid Deficiency (CECD): die Idee, dass ein Mangel an körpereigenen Endocannabinoiden — ähnlich wie Serotoninmangel bei Depression — spezifische Erkrankungen begünstigt oder verursacht.[8]
Erkrankungen, für die eine ECS-Dysfunktion diskutiert wird:
- Migräne: Reduzierte Anandamid-Spiegel in der Cerebrospinalflüssigkeit bei Migränepatienten dokumentiert
- Fibromyalgie: Veränderte CB-Rezeptordichte und Endocannabinoid-Metabolismus nachgewiesen
- Reizdarmsyndrom (IBS): Lokale ECS-Dysregulation in der Darmschleimhaut beschrieben
- Posttraumatische Belastungsstörung (PTBS): Niedrigere AEA-Spiegel mit PTBS-Schwere korreliert
⚠️ Einschränkung: Die CECD-Hypothese ist wissenschaftlich plausibel, aber noch nicht durch kontrollierte klinische Studien bestätigt. Sie bietet einen interessanten konzeptuellen Rahmen — aber noch keine klinische Diagnose oder Therapieempfehlung.
8. Fazit: Warum das ECS der Ausgangspunkt ist
Das Endocannabinoid-System ist kein Zubehör zum Verständnis von CBD — es ist der Ausgangspunkt. Wer CBD verstehen will, muss das ECS kennen: seine Komponenten, seine retrograde Signallogik, seine Verteilung in Haut, Nervensystem und Immunsystem, und die pharmakologische Subtilität, mit der CBD es moduliert — ohne es zu aktivieren oder zu blockieren, sondern indem es die Zeitdauer körpereigener Signale verlängert.
- Das ECS existiert unabhängig von Cannabis. Es wurde durch die Frage entdeckt, warum Cannabis wirkt — aber es ist ein fundamentales Homöostasesystem, das seit Millionen Jahren aktiv ist.
- CBD ist kein direkter Cannabinoid-Rezeptor-Agonist. CBD wirkt primär über FAAH-Hemmung (erhöhtes Anandamid), allosterische CB1-Modulation und Non-CB-Rezeptoren wie TRPV1 und PPARγ.
- CB1 und CB2 haben fundamental unterschiedliche Profile. CB1 im ZNS = psychoaktive THC-Wirkung. CB2 in Haut und Immunsystem = CBD-relevante Hautpflegewirkung.
- Das kutane ECS ist vollständig und autonom. Die Haut besitzt alle ECS-Komponenten und ist ein eigenständiges therapeutisches Zielgewebe für topische CBD-Anwendungen.
🌿 ECS-informierte Hautpflege.
Die CBD-Produkte von MOAR sind auf Basis der in diesem Artikel beschriebenen ECS-Mechanismen entwickelt — mit Vollspektrum-Extrakt für maximale Rezeptorabdeckung und wissenschaftlich fundierter Galenik. Produkte entdecken →
Wissenschaftliche Quellen
- Matsuda, L. A., Lolait, S. J., Brownstein, M. J., Young, A. C., & Bonner, T. I. (1990). Structure of a cannabinoid receptor and functional expression of the cloned cDNA. Nature, 346(6284), 561–564. doi:10.1038/346561a0
- Devane, W. A., Hanus, L., Breuer, A., Pertwee, R. G., Stevenson, L. A., Griffin, G., … & Mechoulam, R. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science, 258(5090), 1946–1949. doi:10.1126/science.1470919
- Munro, S., Thomas, K. L., & Abu-Shaar, M. (1993). Molecular characterization of a peripheral receptor for cannabinoids. Nature, 365(6441), 61–65. doi:10.1038/365061a0
- Wilson, R. I., & Nicoll, R. A. (2001). Endogenous cannabinoids mediate retrograde signalling at hippocampal synapses. Nature, 410(6828), 588–592. doi:10.1038/35069076
- Laprairie, R. B., Bagher, A. M., Kelly, M. E., & Denovan-Wright, E. M. (2015). Cannabidiol is a negative allosteric modulator of delta-9-tetrahydrocannabinol. British Journal of Pharmacology, 172(20), 4790–4805. doi:10.1111/bph.13250
- Bíró, T., Tóth, B. I., Haskó, G., Paus, R., & Pacher, P. (2009). The endocannabinoid system of the skin in health and disease. Trends in Pharmacological Sciences, 30(8), 411–420. doi:10.1016/j.tips.2009.05.004
- Di Marzo, V. (2008). Targeting the endocannabinoid system: to enhance or reduce? Nature Reviews Drug Discovery, 7(5), 438–455. doi:10.1038/nrd2553
- Russo, E. B. (2016). Clinical endocannabinoid deficiency reconsidered. Cannabis and Cannabinoid Research, 1(1), 154–165. doi:10.1089/can.2016.0009
Dieser Artikel dient ausschließlich zu Bildungs- und Informationszwecken. Er stellt keine medizinische Beratung dar. Die beschriebenen Produkte sind keine Arzneimittel.